作者:赵高翔
来源:肿瘤精准医学研究院
编辑:伍恒犁
日期:2025-08-06 阅读:1
新闻网讯 近日,青岛大学肿瘤精准医学研究院在《自然·通讯》(Nature Communications)期刊上发表了题为“Nucleus-translocated glucokinase functions as a protein kinase to phosphorylate TAZ and promote tumour growth”的研究论文,报道了缺氧条件下,肿瘤细胞中的葡萄糖激酶(GCK)发生核转位,在细胞核中通过磷酸化激活Hippo通路关键效应分子TAZ,从而驱动肿瘤细胞的生长。该研究发现了代谢酶GCK具有蛋白激酶的功能,揭示了肿瘤适应不利环境快速生长的重要分子机制。

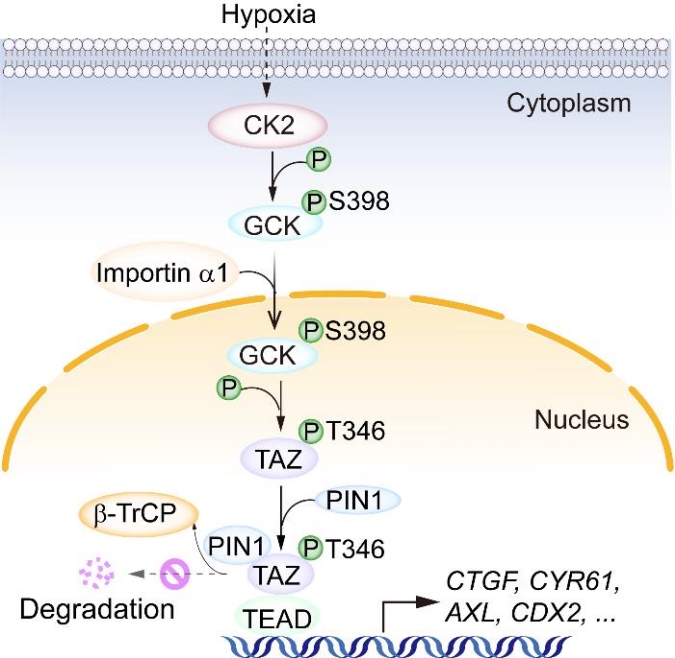
研究人员发现,在缺氧环境中,肿瘤细胞中的酪蛋白激酶2(CK2)会磷酸化GCK的第398位丝氨酸,磷酸化的GCK暴露出其核定位信号序列,并与转运蛋白importin α1结合转移至细胞核内。令人意外的是,传统认知中发挥糖代谢功能的GCK在核内展现出全新的“非经典”功能——作为蛋白激酶直接磷酸化转录共激活因子TAZ的第346位苏氨酸。磷酸化的TAZ结合肽酰脯氨酰异构酶PIN1,引起自身构象的改变,这阻止了泛素连接酶β-TrCP对TAZ的识别,从而抑制了TAZ的降解。稳定的TAZ随后与转录因子TEAD形成复合物,激活细胞增殖和存活等基因的表达,最终促进肿瘤细胞的快速生长。这一发现首次揭示了代谢酶GCK在缺氧条件下通过对Hippo通路的直接调控促进肿瘤生长的重要作用。该研究阐明了GCK作为代谢酶的非代谢酶功能以及“代谢酶-蛋白激酶”角色转换的分子开关机制,为肿瘤治疗策略的制定提供了新思路。
青岛大学为该文第一完成和通讯单位。肿瘤研究院的赵高翔博士为文章第一作者,吕志民教授、方靖教授和邱文生教授为论文的通讯作者。该研究得到国家重点研发计划重点项目、国家自然科学基金、山东省自然科学基金以及青岛市高层次人才计划的资助。
责任编辑:杨伦